生体内での近赤外蛍光タンパク質の高輝度化に成功
〜ビリベルジンレダクターゼノックアウトマウス〜
本研究ではヘム代謝に関与するビリベルジンレダクターゼ(BVR)という酵素をノックアウトしたマウス(Blvra-/-マウス)を作出することで、マウス生体内での近赤外蛍光タンパク質の高輝度化に成功しました。また同様の手法が、近赤外光に応答するカルシウムセンサーや光遺伝学ツールに応用可能であることを示しました。 本研究で作出したBlvra-/-マウスは近赤外光を用いた生体イメージング、および光遺伝学操作において、有用なツールとなることが期待されます。 本研究成果は科学雑誌「Cell Structure and Function」にオンライン掲載されました。
研究の背景
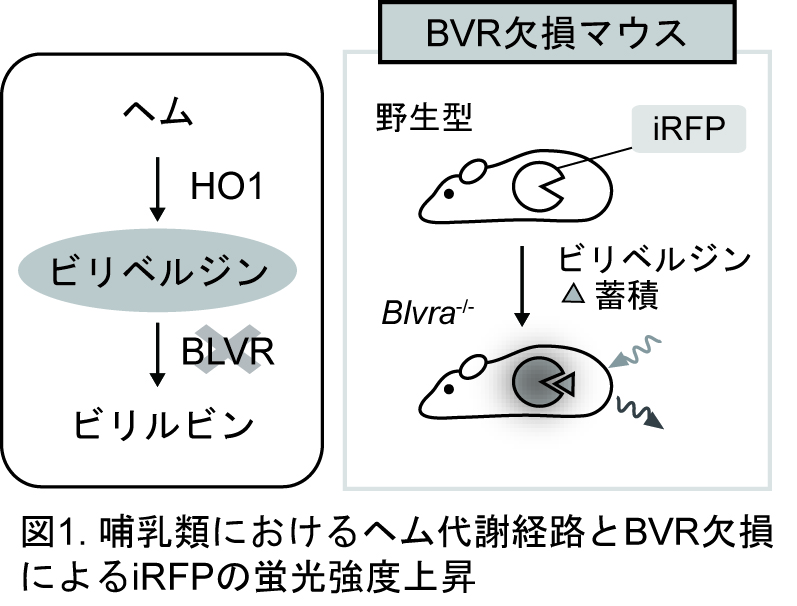
近赤外光を用いた生体イメージングは①高い生体透過性②可視光領域の蛍光タンパク質との併用による多色イメージングという利点から、生体内への応用が望まれてきました。しかしながら、既存の近赤外蛍光タンパク質は蛍光強度が低く、生体への応用は限定されていました。 この理由として、近赤外蛍光タンパク質はビリベルジンというヘム代謝産物を発色団として要求すること、生体内ではビリベルジン濃度が低く保たれていることが原因だと考えられました。
研究の内容と成果
|
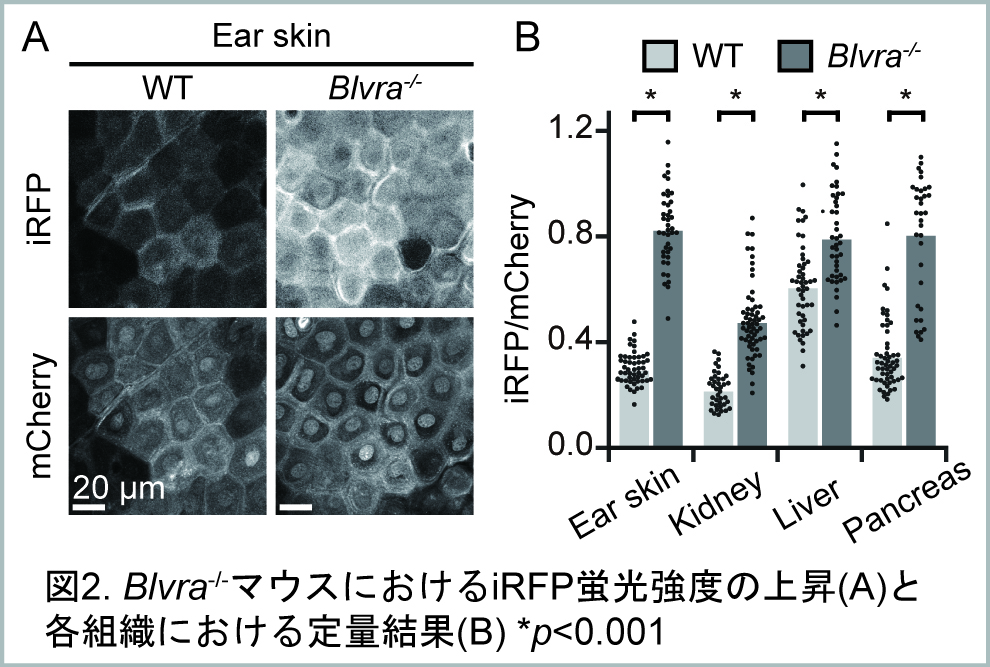
本研究では細胞内のビリベルジン還元酵素をノックアウトしたマウスを作成し、内在性ビリベルジンの濃度を上昇させることで、生体内での近赤外蛍光タンパク質(iRFP)の高輝度化を目指しました(図1)。 多光子顕微鏡を用いてBlvra-/-マウスのiRFP蛍光強度を評価してところ、皮膚、肝臓、腎臓、膵臓において野生型の1.3‾2.8倍となることが分かりました(図2)。 さらに、Blvra遺伝子欠損によりビリベルジンを発色団とする近赤外カルシウムセンサー(NIR-GECO1)が高輝度化すること、 近赤外光遺伝学ツールBphP1システムの光応答性が改善することを示しました。 これらの結果はiRFPをはじめとした近赤外蛍光タンパク質のみならず、近年開発の進む近赤外蛍光バイオセンサー、 および近赤外光遺伝学ツールを生体に応用する際にもBlvra-/-マウスが有用なツールとなることを示すものです。 |
|
研究の意義
本研究で作出したBlvra-/-マウスは近赤外光を用いた生体イメージング、 および光遺伝学操作の基盤技術の一つとなることが期待されます。これによって、生体深部における細胞の動態やシグナル伝達経路の解明に貢献するものと思われます。
今後の展開
現在、Blvra-/-マウスを用いて、生体内での赤色光/近赤外光による光遺伝学操作に取り組んでいます。 我々の研究室で開発しているシアン・黄色蛍光タンパク質 (CFP/YFP)を用いたFRETバイオセンサーを発現するマウスと組み合わせることで、生体内でのシグナル伝達の可視化と操作の両立を目指しています。
用語の解説
- ビリベルジンレダクターゼ:NADH/NADPH依存的にビリベルジンをビリルビンへ還元する酵素
- 光遺伝学:植物、細菌由来の光受容タンパク質を応用し、光によって生命機能を操作する技術。
- 発色団:蛍光タンパク質が蛍光を発するのに必要な原子団。GFPをはじめとしたβ環構造を持つ蛍光タンパク質では内部のアミノ酸残基によって発色団が形成される。 一方で、iRFPをはじめとした近赤外光に応答する蛍光タンパク質の多くは、ビリベルジンなどの小分子を発色団として要求する。
- iRFP:2001年に開発された細菌光受容体由来の近赤外蛍光タンパク質。
- BphP1:細菌由来光受容体タンパク質。近赤外光に応答して結合パートナーのPpsR2とヘテロ2量体を形成することから、 近年、近赤外光遺伝学システムとしての応用が期待されている。
研究プロジェクトについて
科研費および科学技術振興機構戦略的創造研究推進事業(CREST) の支援を受け、実施しました。